تُعرف المادة على أنها أي شيء يشغل حيز في الفضاء وله كتلة، وهي تشغل المكان من حولنا، المواد الصلبة والسائلة أكثر أهمية؛ حيث يمكننا أن نرى أنها تشغل مساحة، ويخبرنا وزنها أن لها كتلة.
الغازات أيضًا مادة وتشغل حيز من الفراغ، وإلا سيظل البالون ساقط بدلاً من الانتفاخ عند ملئه بالغاز.
حالات المادة
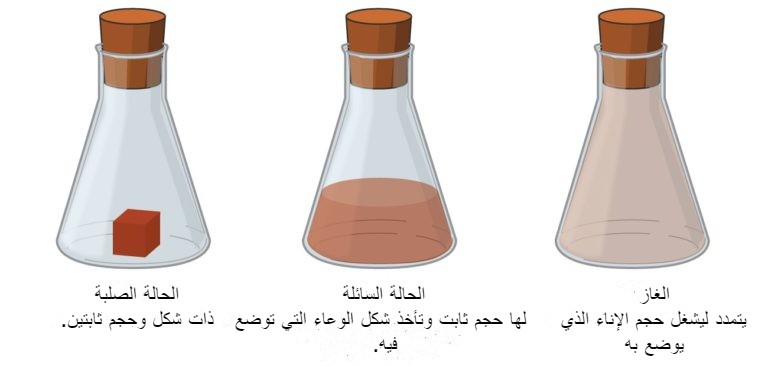
الحالات الثلاث للمادة الشائعة على الأرض: المواد الصلبة والسائلة والغازية (منظر 1).
المواد الصلبة جامده وتمتلك شكلاً محددًا، بينما يتدفق السائل ويتخذ شكل وعاء، باستثناء أنه يشكل سطحًا علويًا مسطحًا أو منحنيًا قليلاً تحت التأثير عليه بواسطة الجاذبية( في انعدام الجاذبية، تتخذ السوائل شكلاً كروياً) تحتوي كل من العينات السائلة والصلبة على أحجام مستقلة جدًا عن الضغط. أما يأخذ الغاز شكل وحجم حاويته.
الحالة الرابعة من المادة هي البلازما، تحدث بشكل طبيعي في التصميمات الداخلية للنجوم.
البلازما هي حالة غازية من المادة تحتوي على أعداد ملحوظة من الجسيمات المشحونة كهربائيًا (منظر 2).
يعطي وجود هذه الجسيمات المشحونة خصائص فريدة للبلازما يجعلها كحالة مادة متميزة عن الغازات.
بالإضافة إلى النجوم، توجد البلازما في بعض البيئات الأخرى ذات درجات الحرارة العالية (سواء الطبيعية أو من صنع الإنسان)، مثل الصواعق وبعض شاشات التلفزيون والأدوات التحليلية المتخصصة المستخدمة لاكتشاف الكميات الضئيلة من المعادن.

في خلية صغيرة في تلفزيون البلازما، تُصدر البلازما الضوء فوق البنفسجي، مما يؤدي بدوره إلى ظهور الشاشة في ذلك الموقع بلون معين، تجميع هذه النقاط الصغيرة من الألوان يشكل الصورة التي تراها.
يبدو أن بعض عينات المادة لها خصائص المواد الصلبة والسوائل و / أو الغازات في نفس الوقت. يمكن أن يحدث هذا عندما تتكون العينة من العديد من القطع الصغيرة؛ على سبيل المثال، يمكننا صب الرمل كما لو كان سائلًا لأنه يتكون من العديد من الحبيبات الصغيرة من الرمل الصلب.
يمكن أن يكون للمادة أيضًا خصائص لأكثر من حالة واحدة عندما تكون خليطًا، مثل السُحب.
يبدو أن السُحب تتصرف إلى حد ما مثل الغازات، لكنها في الواقع عبارة عن خليط من الهواء (الغاز) وجزيئات صغيرة من الماء (سائلة أو صلبة).
الكتلة والوزن
كتلة أي شيء هي مقياس لكمية المادة الموجودة فيه، إحدى طرق قياس كتلة الجسم هي قياس القوة اللازمة لتسريع الجسم.
إن تسريع السيارة يتطلب قوة أكبر بكثير مما تتطلبه الدراجة لأن كتلة السيارة أكبر بكثير، الطريقة الأكثر شيوعًا لتحديد كتلة جسم هي استخدام ميزان لمقارنة كتلته بالكتلة المعيارية.
وعلى الرغم من أن الوزن مرتبط بالكتلة، إلا أنه ليس نفس الشيء؛ حيث يشير الوزن إلى القوة التي تؤثر بها الجاذبية على جسم ما؛ هذه القوة تتناسب طرديًا مع كتلة الجسم، يتغير وزن الجسم مع تغير قوة الجاذبية، لكن كتلته لا تتغير.
لا تتغير كتلة رائدة الفضاء لمجرد ذهابها إلى القمر؛ ولكن وزنها على القمر سدس وزنها على الأرض لأن جاذبية القمر تساوي سدس وزن الأرض.
قانون بقاء المادة
يلخص قانون بقاء المادة العديد من الملاحظات العلمية حول المادة: فهو ينص على أنه لا يوجد تغيير يمكن اكتشافه في الكمية الكلية للمادة الموجودة عندما تتحول المادة من نوع إلى آخر (تغيير كيميائي) أو تغيرات في الحالة الصلبة أو السائلة أو الغازية (تغيير فيزيائي).
يقدم تخمير البيرة وتشغيل البطاريات أمثلة على الحفاظ على المادة (منظر 3)، أثناء تخمير البيرة، تتحول المكونات (الماء، والخميرة، والحبوب، والشعير، والقفزات، والسكر) إلى بيرة (ماء، كحول، كربونات، ونكهات مواد ) دون فقد فعلي للمادة، يتضح هذا أثناء عملية التعبئة، عندما يتحول الجلوكوز إلى إيثانول وثاني أكسيد الكربون، ولا تتغير الكتلة الكلية للمواد.
يمكن ملاحظة ذلك أيضًا في بطارية السيارة الرصاص الحمضية: تتغير المواد الأصلية (الرصاص وأكسيد الرصاص وحمض الكبريتيك) القادرة على إنتاج الكهرباء إلى مواد أخرى (كبريتات الرصاص والماء) لا تنتج الكهرباء، مع عدم وجود تغيير في المقدار الفعلي للمادة.
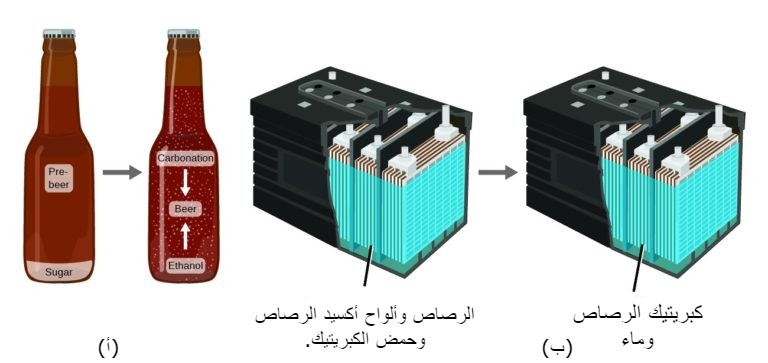
(ب) تكون كتلة الرصاص وألواح أكسيد الرصاص وحمض الكبريتيك التي تدخل في انتاج الكهرباء مساوية تمامًا لكتلة كبريتات الرصاص والماء المتكون.
على الرغم من أن قانون الحفظ هذا ينطبق على جميع تحويلات المادة، إلا أن الأمثلة المقنعة قليلة ومتباعدة؛ لأننا خارج الظروف الخاضعة للرقابة في المعمل، نادرًا ما نجمع كل المواد التي تنتُج أثناء تحويل معين؛ على سبيل المثال، عندما تأكل، وتهضم الطعام، تحفظ كل المواد الموجودة في الطعام الأصلي.
ولكن نظرًا لدمج بعض هذه المواد في جسمك، وإفراز الكثير منها على شكل أنواع مختلفة من النفايات، فمن الصعب التحقق من ذلك عن طريق القياس.
الخواص الفيزيائية والكيميائية للمواد
الخواص الفيزيائية
الصفات التي تمنحنا التمييز- التفرقة – بين المادة وغيرها تسمي الخواص. الخاصية الفيزيائية هي صفة للمادة لا ترتبط مع تغيرات في تركيبها الكيميائي.
الأمثلة المعروفة بالنسبة للخواص الفيزيائية تشمل:
- الكثافة
- اللون
- الصلابة
- درجتي الغليان
- الذوبان
- التوصيل الكهربي
يمكننا أن نلاحظ بعض الخواص الفيزيائية مثل الكثافة واللون دون تغير في الحالة الفيزيائية للمادة، بينما الخواص الفيزيائية الأخرى مثل درجة انصهار الحديد ودرجة تجمد المياه لا يمكننا ملاحظتها لأن المادة تكون تحت تأثير تغير فيزيائي.
التغير الفيزيائي: هو تغير في حالة أو خواص المادة دون تغير مصاحب في تركيبها الكيميائي. ’
نلاحظ التغير الفيزيائي عندما يذوب الشمع، عندما يذوب السكر في القهوة، وعندما يتكثف البخار ويتحول الي مياه (منظر ٤).
أمثلة اخري للتغير الفيزيائي تشمل مغناطيسية وعدم مغناطيسية المعادن؛’كما هو شائع في الحمالات الأمنية( تفتيت – طحن – المعادن إلى مساحيق،التي يصحبها تغير ملحوظ في اللون أحيانًا).
في كل هذه الأمثلة هناك تغير في الحالة الفيزيائية، التكوين، أو خواص المادة، لكن ليس هناك تغير في التركيب الكيميائي للمادة.

الخواص الكيميائية
تغير المادة من نوع إلى آخر’أو عدم القدرة علي التغير يُعد خاصية كيميائية.
تشمل الأمثلة على الخواص الكيميائية:
- قابلية الاشتعال
- السمية
- الحامضية
- النشاط الكيميائي
- حرارة المواد القابلة للاحتراق
علي سبيل المثال، الحديد عندما يتواجد مع الأكسجين في وجود الماء يتكون الصدأ، بينما الكروم لا يتأكسد (منظر ٥ ). النيتروجلسرين خطير جدًا حيث إنه ينفجر بسهولة، غاز النيون لا يشكل أي خطورة لأنه غير نشط للغاية.

التغير الكيميائي: يُنتج دائمًا نوع أو أكثر من المواد التي تختلف عن المادة الموجودة قبل التغير. تكّون الصدأ هو تغير كيميائي لأن الصدأ نوع مختلف عن مادة الحديد، مع وجود الأكسجين والماء قبل تكون الصدأ.
انفجار النيتروجلسرين هو تغير كيميائي لأن الغازات الناتجة نوع مختلف تمامًا عن المادة الأصلية.
ومن الأمثلة الأخرى عن التغير الكيميائي التفاعلات الذي تحدث في المعمل مثل(منظر ٦)؛
- تفاعل النحاس مع حمض النيتريك لتكوين نترات النحاس، وأبخرة النيتروز البينية، وغاز ثاني أكسيد النيتروجين.
- تفاعلات الاحتراق؛ احتراق عود الثقاب، تتفاعل الخلايا في العود والأكسجين من الهواء تحت تأثير التغير الكيميائي لتكوين ثاني أكسيد الكربون وبخار الماء.
- والطعام المطهي؛ طهي اللحوم الحمراء يسبب عدد من التغيرات الكيميائية تشمل أكسدة الحديد في الهيموجلوبين والذي ينتج عنها التحول المعتاد من اللون الأحمر إلى اللون البني.
- الطعام المُعفن.
- تحول الموز إلى اللون البني يعد تغييرًا كيميائيًا حيث تتكون مواد جديدة أغمق.

تندرج خواص المادة تحت واحدة من فئتين.
إذا كانت الخاصية تعتمد علي كمية المادة الموجودة، تكون خاصية شاملة، كتلة وحجم المادة أمثلة للخواص الشاملة؛ في حالة دورق الحليب يكون أكبر في الكتلة والحجم من كوب الحليب. تتناسب قيمة الخاصية الشاملة بشكل مباشر مع كمية المادة المحددة.
إذا كانت خاصية عينة من المادة لا تعتمد علي مقدار المادة الموجودة، تكون خاصية مكثفة.
الحرارة هي المثال علي الخاصية المكثفة؛ إذا كان هناك دورق وكأس من الحليب كلاهما عند نفس درجة حرارة الغرفة 20 درجة مئوية عندما يندمجان، درجة الحرارة تبقي 20 درجة مئوية.
مثال آخر، ضع في اعتبارك الخصائص المميزة؛ ولكن ميّز بين الحرارة ودرجة الحرارة، إذا سقط زيت مغلي وانتشرت علي ذراعك قطرات طفيفة، تشعر بعدم راحة، بينما إذا سقط إناء من زيت ساخن ينتج عنة حروق خطيرة. كل من القطرة أو الإناء في نفس درجة الحرارة( خاصية مكثفة)؛ ولكن الإناء بالطبع يكون أكثر سخونة( خاصية شاملة).
الماس الخطر
قد رأيت العنوان الموضح في (منظر ٧) بشأن عبوات المواد الكيميائية في المعمل أو ورشة العمل، أحيانًا يسمى”ماسة النار” أو “خطر الماس”هذا الماس الخطر يوفر معلومات قيمة مختصرة عن المخاطر المختلفة الذي يجب إدراكها عند العمل بمادة معينة.
معيار الرابطة الوطنية للوقاية من الحرائق(NFPA) رقم 470، يتطور نظام تحديد المخاطر بواسطة(NFPA) لكي يوفر المعلومات الآمنة عن بعض المواد؛ من تفاصيل النظام: المواد القابلة للاشتعال، التفاعلات، السلامة، بعض المخاطر الأخرى.
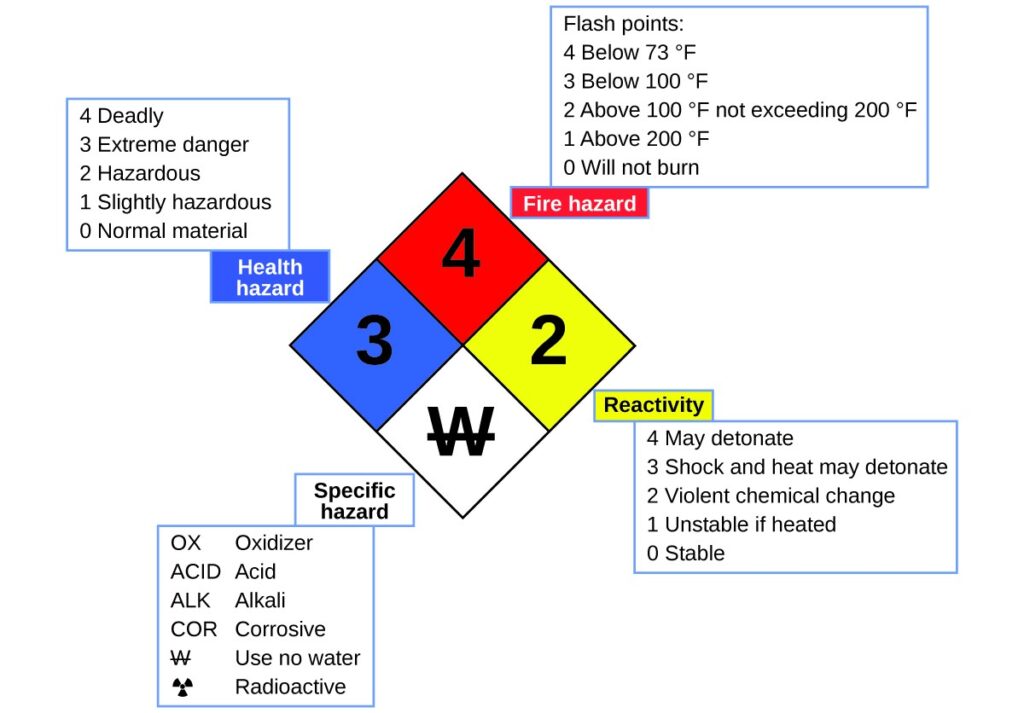
الرموز الكلية للماس
- ” الحمراء”:في القمة المخاطر، الماس هنا يحدد مستوى خطورة الحرائق( نقاط درجة الحرارة في اهم النقاط).
- ” الأزرق: في اليسار الماس يشير إلى مستوى سلامة الحرائق.
- “الأصفر :في اليمين، يصف تفاعلية المخاطر مثل؛ مدي سهولة خضوع المادة للتفجير أو التغيير الكيميائي العنيف.
- ” الابيض”: في القاع يشير الى مخاطر خاصة مثل؛ إذا كانت المادة مؤكسدة( السماح للمادة بالاحتراق في وجود الأكسجين/ الهواء) أو تخضع المادة لتغير غير مألوف أو خطير عندما تتفاعل مع الماء، وتكون مادة آكلة وحامضية و قاعدية وخطر حيوي ومشع.
- ما هو التغيير الكيميائي؟ التغير الناتج عن نوع مختلف من المواد عن النوع الأصلي من المواد.Add Image
- ما هي الخاصية الكيميائية؟ السلوك المرتبط بتغيير نوع من المواد إلى نوع آخر من المواد.Add Image
- ما هي الخاصية الشاملة: الخاصية التي تعتمد على كمية المادة.Add Image
- ما هي الخاصية المكثفة؟ الخاصيةالمستقلة عن كمية المادة.Add Image
المصادر
- Phases and Classification of Matter من موقع “coursehero”
ما هي حاالات المادة؟
تصنف المواد إلى صلبة وسائلة وغازية وهي التي تقابلنا في الحياة اليومية، بالإضافة إلى الحالة الرابعة، البلازما.
ما الفرق بين الكتلة والوزن؟
الكتلة هي مقدار ما يحتويه الجسم من مادة؛ بينما الوزن هو قوة جذب الأرض للجسم وتتأثر بيغيير المكان على عكس الكتلة.
قانون بقاء المادة أو الكتلة.
أثناء التفاعل الكيميائي، كتل المواد المتفاعلة تكون مساوية لكتل المواد الناتجة.
ما هو التغيير الكيميائي؟
التغير الناتج عن نوع مختلف من المواد عن النوع الأصلي من المواد.
ما هي الخاصية الكيميائية؟
السلوك المرتبط بتغيير نوع من المواد إلى نوع آخر من المواد.
ما هي الخاصية الشاملة:
الخاصية التي تعتمد على كمية المادة.
ما هي الخاصية المكثفة؟
الخاصيةالمستقلة عن كمية المادة.






