يعرف معظم الناس كلمات حمض أو حامضي؛ بسبب المطر الحمضي -الذي يعد من أخطر المشكلات البيئية التي تواجه العالم بسبب معدل حموضته المرتفعة- أو الأطعمة الحمضية، مثل عصير الليمون.
ومع ذلك فإن قلة من الناس على دراية بنقيض الحمض؛ القاعدة (وتسمي أيضًا القلوية) وتتضمن المواد القاعدية مثل:
- الصابون
- وصودا الخبز (بيكربونات الصوديوم)
مقياس الأس الهيدروجيني (PH)
تعبّر قيمة الأس الهيدروجيني (pH) عن مقدار تركيز أيونات الهيدروجين (H+) في سائل معين.
إذا كان تركيز أيونات الهيدروجين (H+) في السائل مرتفعًا، فإنه يكون حمضيًا وإذا كان التركيز منخفضًا، فإنه يكون قاعديًا (قلويًا).
وهذا يعني أنه عند قياس تركيز أيونات الهيدروجين يمكن معرفة مقدار الحموضة والتعادل والقلوية، وكذلك درجة كل منها.
يتراوح مقياس الأس الهيدروجيني من صفر إلى أربعة عشر ويمكن قياسه بوسطة ورق عباد الشمس.
ورقة عباد الشمس: هي خليط من صبغات قابل للذوبان في الماء، تُستخلص من النباتات (الأشناته وخاصة روسلا تينكوتوريا)، وتمتص بواسطة ورقة ترشيح، تستخدم كمؤشر لقياس حمضية المواد.
يتحول لون ورقة عباد الشمس الزرقاء للأحمر عند تعرضها لحمض، كما يتحول لون ورقة عباد الشمس الحمراء للأزرق عند تعرضها لمادة قاعدية(قلوية).

اختبار الأس الهيدروجيني:
يقيس هذا الاختبار كمية أيونات الهيدروجين الموجودة في محلول معين.
ينتج عن التركيزات العالية من أيونات الهيدروجين في محلول معين درجة حموضة عالية (PH منخفضة)، بينما تؤدي التركيزات المنخفضة من أيونات الهيدروجين إلى انخفاض درجة الحموضة (PH عالية مادة قاعدية).
وبالتالي يتناسب تركيز أيونات الهيدروجين عكسيًا مع قيمة الأس الهيدروجيني.
يمثل تغير درجة واحدة على مقياس الأس الهيدروجيني تغير في تركيز أيونات الهيدروجين بمعدل ١٠، والتغير في وحدتين يمثل تغير في تركيز أيونات الهيدروجين بمعدل ١٠٠؛ وبالتالي التغيرات الطفيفة في الرقم الهيدروجيني تمثل تغيرات كبيرة في تركيز أيونات الهيدروجين.
قيمة الأس الهيدروجيني:
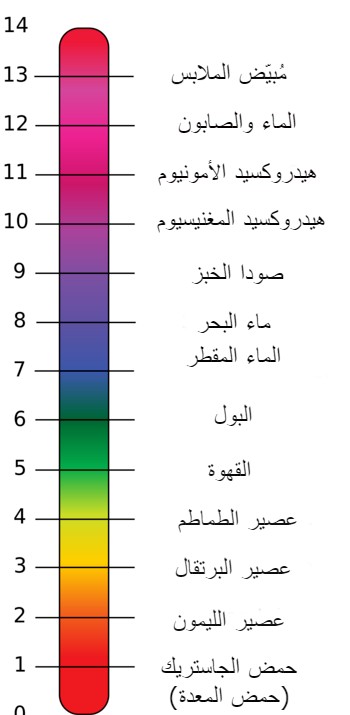
الرقم الهيدروجيني الأقل من 7 يكون حامضيًا، والأكبر من 7 يكون قلويًا، ويكون متعادلًا عندما يساوي 7.
فيما يلي قيمة الأس الهيدروجيني لبعض المواد:
- الدم: يعتبر قاعدة ضعيفة (الرقم الهيدروجيني =٧,٤)
- البيئة في معدتك: تعتبر شديدة الحموضة (الرقم الهيدروجيني = ٢:١)
- عصير البرتقال: يعتبر حامضي (الرقم الهيدروجيني = ٣,٥)
- صودا الخبز: تعتبر قاعدية (الرقم الهيدروجيني = ٩)
الحمض: المادة التي تعطي أيون الهيدروجين الموجب (+H) عند انحلالها في الماء، وبالتالي يقلل قيمة الأس الهيدروجيني ( PH ).
القاعدة: المادة التي تعطي أيون الهيدروكسيد السالب–(HO) عند انحلالها في الماء، وترتفع قيمة الأس الهيدروجيني (PH).
الحمض القوي: هو الحمض الذي يتفكك بشكل كامل في الماء، ويعطي أيون الهيدروجين الموجب +H، مثل: حمض الهيدروكلوريك.
القاعدة القوية: هي التي تتفكك بشكل كامل في الماء، وتعطي أيون الهيدروكسيد السالب−(OH)، مثل: هيدروكسيد الصوديوم، وكربونات الصوديوم.
المحاليل المنظمة
تعمل معظم الخلايا في أجسامنا ضمن نطاق ضيق جدًا من الأس الهيدروجيني عادة ما يتراوح من (٧,٢: ٧,6)
إذا كان الرقم الهيدروجيني خارج النطاق المحدد، سيحدث خلل في جميع أجهزة الجسم بحيث:
- لن تعمل الخلايا بشكل جيد.
- البروتينات ستتفكك.
- وممكن أن تؤدي إلى غيبوبة أو وفاة.
والسؤال؛ كيف يمكننا أن نبتلع أو نستنشق المواد الحامضية أو القاعدية دون الموت؟
المحاليل المنظمة هي المفتاح؛ تمتص الزيادة من أيون الهيدروجين الموجب أو أيون الهيدروكسيد السالب بعناية للحفاظ على درجة الحموضة في الجسم.
بعض الأمثلة على المحاليل المنظمة داخل جسم الإنسان:
- ثاني أوكسيد الكربون: جزء من المحلول المنظم في جسم الإنسان يحافظ على الرقم الهيدروجيني ضمن نطاق مناسب.
- حمض الكربونيك.
- أيونات البيكربونات.
حمض الكربونيك كمحلول منظم
عند زيادة تركيز أيون الهيدروجين الموجب عن النطاق المناسب؛ يتحد أيون البيكربونات مع أيون الهيدروجين الموجب لتكوين حمض الكربونيك وبالتالي نتجنب الانخفاض في قيمة الرقم الهيدروجيني،
عند زيادة تركيز أيون الهيدروكسيد السالب الداخل إلى الجسم، يتفكك حمض الكربونيك إلى بيكربونات وأيون الهيدروجين الذي يتحد مع أيون الهيدروكسيد؛ مكونًا ماء وبالتالي؛ حمض الكربونيك يحد من الزيادة في قيمة الرقم الهيدروجيني.
أهمية حمض الكربونيك في الجسم
سريع الزوال؛ إذ ينطلق من الجسم كغاز ثاني أوكسيد الكربون في كل مرة نتنفس فيها، فبدون هذا المحلول المنظم سيتذبذب الأس الهيدروجيني في أجسامنا، وستكون احتمالية البقاء على قيد الحياة ضعيفة.
أي مقياس من صفر إلى 14 يُستخدم لقياس الحموضة أو القلوية؟
القيمة 7 هي المستوى المتعادل، إذا قلت القيمة عن 7 يعني هذا زيادة الحموضة وإذا اذدادت عن 7 تزداد القلوية.
ما هي المحاليل المنظمة؟
المحاليل التي تقاوم التغير في الرقم الهيدروجيني عند إضافة كميات قليلة من الأحماض أو القواعد القوية أو عند تخفيفها
اذكر أمثلة على المواد القاعدية؟
صودا الخبز، الصابون.






